
Кристалічні та аморфні стани (частина ІІ)
Доброго дня! В продовження теми про будову та властивості речовин, сьогодні поговоримо про вплив хімічної будови на утворення твердого стану речовини.
Кожного дня ми з вами стикаємося з великою кількістю різноманітних речовин. Навчилися їх використовувати у своєму повсякденному житті. І рідко задаємося запитанням, чому одні з них гази, інші рідини чи тверді речовини.
З попередньої теми знаємо, що агрегатний стан речовин залежить від типів хімічного зв'язку в молекулах речовин та від міжмолекулярної взаємодії. А ще знаємо, що молекулярну будову мають далеко не всі речовини.
Твердим речовинам притаманні два стани: кристалічний та аморфний.
Йонний тип хімічного зв'язку характерний для солей. Багато речовин мають кристали - самоутворені тверді тіла з плоскими гранями та прямими ребрами. Найпростішим прикладом речовини з кристалічною будовою є кухонна сіль (натрію хлорид NaCl). А ще ми всі знаємо про коштовні камені (гранати, рубіни, алмази ...), які теж утворюють кристали. Вільний кремній утворює і кристали, і аморфну масу.

Внутрішня структура (скелет) кристала — кристалічна ґратка. Ґратки кристалів бувають різних типів: йонні, молекулярні, атомні, металічні. Тип ґратки залежить від того з яких найменших частинок, що у вузлах ґратки, утворилася речовина.
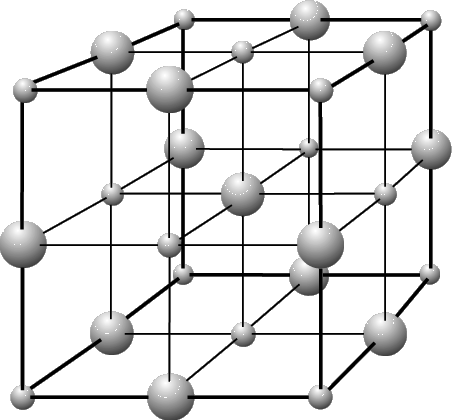
В кристалічному стані за звичайних умов або при низьких температурах перебуває більшість простих речовин, неорганічних сполук. І навіть органічні речовини, яких невеликі молекули (глюкоза, фруктоза).
Але серед твердих речовин є й такі у яких внутрішня структура немає такого чіткого впорядкування. Найдрібніші їх частинки (атоми, молекули) розміщуються хаотично і за такою особливістю вони швидше нагадують рідини, а не тверді речовини. Це аморфні речовини.
Якщо вам "повезло" в дитинстві (чи не в дитинстві ☺) розбити скляну вазу чи стакан, ви помічали, що "розлітаються" вони на велику кількість друзок, осколків різної форми. Так виглядають аморфні речовини. Найгарнішим прикладом аморфної речовини можна навести воду в твердому стані — сніжинки. Вони зачаровують різноманітністю форм та розмірів. Кожна сніжинка не схожа на іншу, особлива, унікальна ☺. Чому?

В аморфних речовинах, як і в рідинах, впорядковані лише частинки, що розміщуються поряд. У віддалені — порядок втрачається.
До аморфних речовин належать вищі карбонові кислоти, полісахариди, білки, жири, багато синтетичних полімерів, а також скло та бурштин. Цікаво знати, що аморфними є й деякі метали (металічне скло Au75Si25). Вперше отримане у 1960 році в Каліфорнійському технологічному університеті.
Не дивлячись на те що, кристалічні та аморфні речовини є твердими, вони відрізняються за фізичними властивостями. Так при нагріванні кристалічної речовини, вона починає розкладатися за певної температури ( Al — 660 °С, алмаз — 3827 °С), а речовина аморфна плавиться в певному діапазоні температур і стає в'язкою, що дозволяє виготовляти з неї вироби різної форми (тут згадаємо пластилін з якого діти ліплять різні фігурки, попередньо розігрівши матеріал в долоньках☺).
Оптичні властивості та твердість кристалічних речовин залежать від напрямку дії сили та напрямку променя світла, а в аморфних — ні.
У даній темі є багато цікавого. Так, скажімо, хімія рідких кристалів чи аморфних металів. Цікаві презентації-доповіді про які я чекаю від своїх студентів☺.
Домашнє завдання: підручник Попель, Крикля для 11 класу §8; вправи 65, 66 сторінка 48. Творча робота: презентації про рідкі кристали, або металічне скло.




